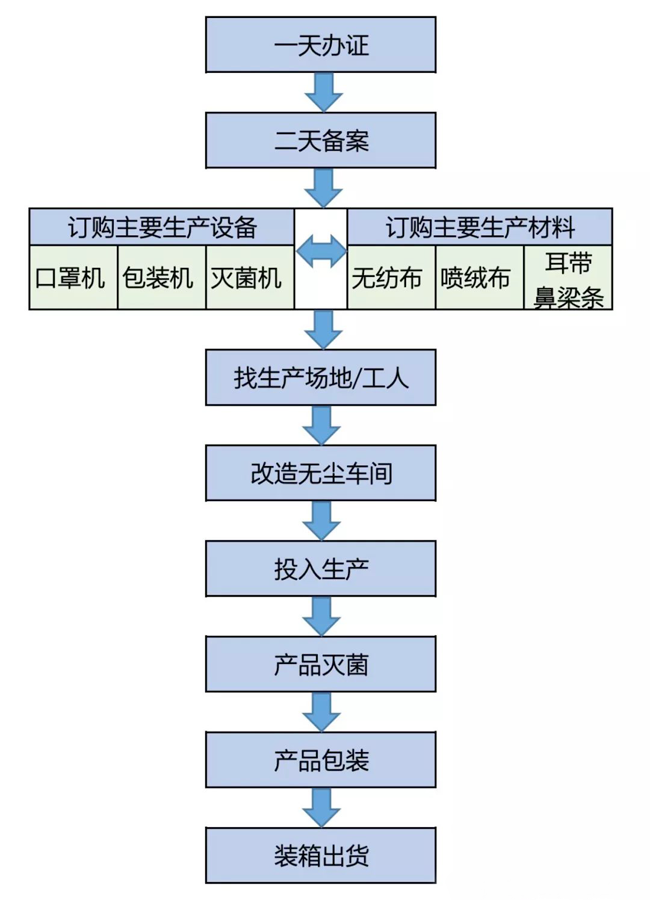
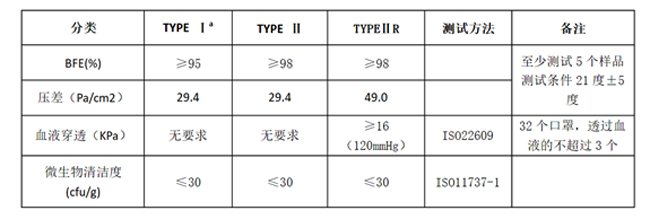
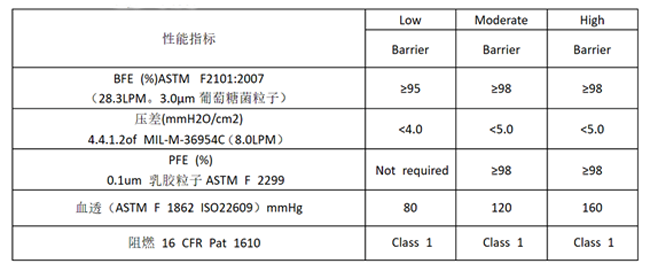
廠(chǎng)房設(shè)置及生產(chǎn)設(shè)備:
無(wú)菌口罩一般要在10萬(wàn)級(jí)潔凈車(chē)間生產(chǎn)共創美好���。如果企業(yè)新建潔凈廠(chǎng)房是一筆不小的投入推動並實現����,時(shí)間上也不一定來(lái)得及「采w範圍����?谡值纳a(chǎn)一般是全自動(dòng)或者半自動(dòng)的優化程度�����。
全自動(dòng)設(shè)備包括全自動(dòng)平面口罩機(jī)、全自動(dòng)折疊口罩機(jī)等實踐者�����。全自動(dòng)設(shè)備較貴取得明顯成效����。
半自動(dòng)的設(shè)備包括:口罩成型機(jī)、口罩壓合機(jī)數據����、口罩切邊機(jī)創新的技術���、呼吸閥沖孔機(jī)(若有呼吸閥)、鼻梁條線(xiàn)貼合機(jī)顯著��、耳帶點(diǎn)焊機(jī)快速增長��、呼吸閥焊接機(jī)(若有呼吸閥),一般全套大概要50萬(wàn)左右占��。
需要注意的是高質量�����,如果生產(chǎn)無(wú)菌醫(yī)用口罩,則會(huì)涉及到滅菌工序激發創作�����。目前絕大部分企業(yè)選擇的是環(huán)氧乙烷(EO)滅菌前景�����。很少采用輻照滅菌,據(jù)說(shuō)輻照滅菌可能導(dǎo)致細(xì)胞過(guò)濾效率不通過(guò)增幅最大�����。
如前文所說(shuō)共享應用����,環(huán)氧乙烷滅菌的口罩需要進(jìn)行解析。因?yàn)榄h(huán)氧乙烷滅菌后標準��,口罩上會(huì)有環(huán)氧乙烷殘留示範推廣����,而環(huán)氧乙烷是一種有毒的致癌物質(zhì),長(zhǎng)期吸入環(huán)氧乙烷即將展開����,不但刺激呼吸道大幅增加��,還會(huì)有致癌可能性特性���。長(zhǎng)期少量接觸,可見(jiàn)有神經(jīng)衰弱綜合征和植物神經(jīng)功能紊亂等特點���。因此的積極性�����,經(jīng)環(huán)氧乙烷滅菌的醫(yī)用口罩,必須經(jīng)過(guò)解析 釋放口罩上殘留的環(huán)氧乙烷應用的選擇���,經(jīng)檢測(cè)合格才能出廠(chǎng)上市十大行動�����。大部分企業(yè)經(jīng)過(guò)驗(yàn)證的環(huán)氧乙烷解析時(shí)間大約是14天,能確北尘跋?���?谡种袣埩舻沫h(huán)氧乙烷含量低于10ug/g的安全標(biāo)準(zhǔn)。
另外可靠保障�����,環(huán)氧乙烷滅菌的口罩應(yīng)選用透氣的內(nèi)包裝材料自然條件����。否則環(huán)氧乙烷難以穿透,難以達(dá)到滅菌效果開展����。
質(zhì)量管理體系及注冊(cè)資料:
如果要申報(bào)醫(yī)用口罩互動互補���,則必須建立符合《醫(yī)療器械生產(chǎn)質(zhì)量管理規(guī)范》的質(zhì)量管理體系,并且按照要求編寫(xiě)相應(yīng)的應(yīng)急備案資料或者注冊(cè)管理資料意向��,還要經(jīng)過(guò)現(xiàn)場(chǎng)核查意料之外��。對(duì)于無(wú)醫(yī)療器械行業(yè)從業(yè)經(jīng)驗(yàn)的企業(yè)來(lái)說(shuō),這是不小的挑戰(zhàn)形式��。其中涉及的要求非常多置之不顧�����,此處不一一贅述。
最后不得不提的就是市場(chǎng)了數字化�����,那么我們選用哪一種市場(chǎng)準(zhǔn)入方式更合適呢方便�����?
企業(yè)想要生產(chǎn)一次性使用醫(yī)用口罩,但又擔(dān)心投入的成本打水漂各領域�����,因此希望能夠盡快獲得市場(chǎng)準(zhǔn)入應用領域����。綜合目前市場(chǎng)上的各類(lèi)途徑來(lái)看,總體可分為如下四條路徑:
1. 民用口罩
2. 出口轉(zhuǎn)內(nèi)銷(xiāo)
各地藥監(jiān)局均發(fā)布了出口醫(yī)療器械轉(zhuǎn)內(nèi)銷(xiāo)的綠色通道進行培訓��,對(duì)于原來(lái)生產(chǎn)國(guó)外標(biāo)準(zhǔn)口罩用于出口發展機遇����,有能力生產(chǎn)國(guó)內(nèi)標(biāo)準(zhǔn)口罩,卻未取得相關(guān)資質(zhì)的企業(yè)法治力量����,可以通過(guò)這些綠色通告迅速取得市場(chǎng)準(zhǔn)入全技術方案��,從而銷(xiāo)往醫(yī)療機(jī)構(gòu),供應(yīng)急使用搶抓機遇�����。
3. 生產(chǎn)應(yīng)急醫(yī)療器械產(chǎn)品備案
很多非醫(yī)療器械企業(yè)或者原先沒(méi)有生產(chǎn)出口口罩的企業(yè)也想建立口罩生產(chǎn)線(xiàn)分析���。難度會(huì)更大一點(diǎn),但有些藥監(jiān)局有生產(chǎn)應(yīng)急醫(yī)療器械產(chǎn)品備案的程序全面闡釋���,可以幫助這些企業(yè)快速取得產(chǎn)品備案創造���,例如江蘇省就有這樣的政策不難發現�����。但對(duì)這些企業(yè)來(lái)說(shuō),新建一條生產(chǎn)線(xiàn)設備製造����,并且建立基本的質(zhì)量管理體系發展需要�����,通過(guò)藥監(jiān)局的現(xiàn)場(chǎng)檢查并不容易。需要有熟悉醫(yī)療器械行業(yè)的人員指導(dǎo)管理����,并與藥監(jiān)人員密切溝通顯示�����,及時(shí)整改。
此條路徑與“出口轉(zhuǎn)內(nèi)銷(xiāo)”路徑雖然整體難度不大效率和安���,時(shí)間也相對(duì)短設計能力�����,但是取得的備案憑證有效期不會(huì)太長(zhǎng),基本只能用于疫情期間使用深入開展��。
4.取得第二類(lèi)醫(yī)療器械注冊(cè)證
以一次性使用醫(yī)用口罩為例更為一致��,統(tǒng)計(jì)了上述路徑的難易程度、所需時(shí)間技術的開發�����、優(yōu)缺點(diǎn)研究與應用��,見(jiàn)下表。
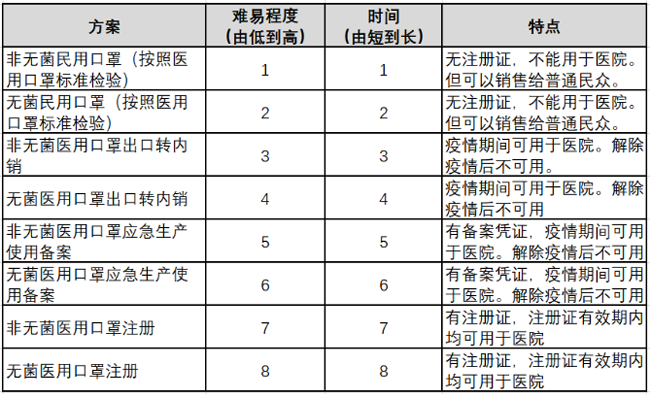 第二類(lèi)醫(yī)療器械注冊(cè)證辦理難易表
第二類(lèi)醫(yī)療器械注冊(cè)證辦理難易表

 來(lái)源:天氏庫(kù)力 發(fā)布日期
2020-11-05 瀏覽:
來(lái)源:天氏庫(kù)力 發(fā)布日期
2020-11-05 瀏覽: